Лікування хронічного мієлолейкозу (ХМЛ) було революційно змінено завдяки інгібіторам тирозинкінази (ІТК), перетворивши колись смертельне захворювання на керований хронічний стан. В основі цієї історії успіху лежить точний та надійний моніторингГен злиття BCR-ABL—визначальний молекулярний фактор розвитку ХМЛ.
Окрім початкового діагнозу, кількісне визначення BCR-ABL є основою ефективного довічного ведення пацієнтів. Воно надає клініцистам критично важливі дані, необхідні для:
Встановлення базової лініїпри постановці діагнозу.
Оцінка ранньої відповіді на лікуваннята прогнозувати довгострокові результати.
Керівництво з коригування терапії TKIна основі етапів молекулярної відповіді.
Монітор мінімальної залишкової хвороби (MRD)та потенційний рецидив.
Однак,Ненадійне виявлення може поставити під загрозу ці рішення.
Макро- та мікротестування's Набір для виявлення мутацій генів злиття людського BCR-ABLрозроблений для забезпечення точності, необхідної для впевненості на кожному етапі.
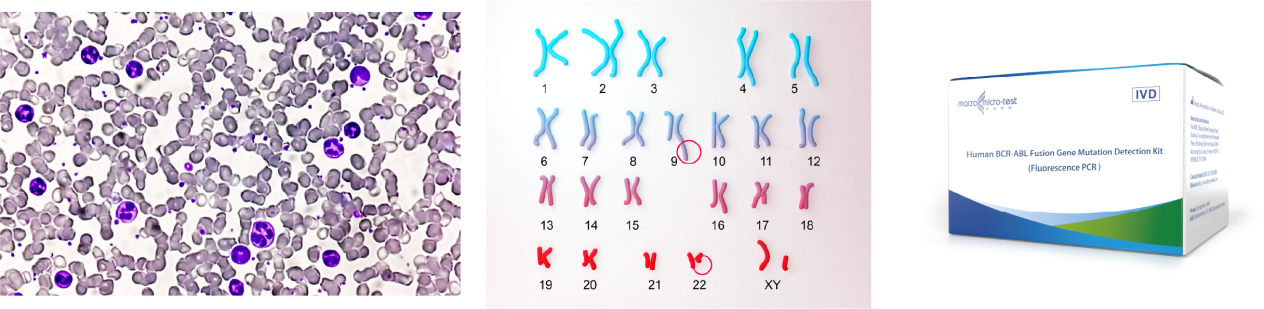

Чому наше рішення є надійним партнером у лікуванні ХМЛ:
- Комплексне профілювання:Одночасно виявляє три основні транскрипти BCR-ABL (P210, P190, P230), гарантуючи, що жоден критичний випадок не буде пропущено.
- Неперевершена чутливість:Досягає межі виявлення (LoD) до1,000 копій/мл, що дозволяє ранню та точну оцінку глибоких молекулярних відповідей.
- Сувора точність:Включає систему внутрішнього контролю та ферментів UNG для усунення хибнопозитивних/негативних результатів, захищаючи цілісність результатів.
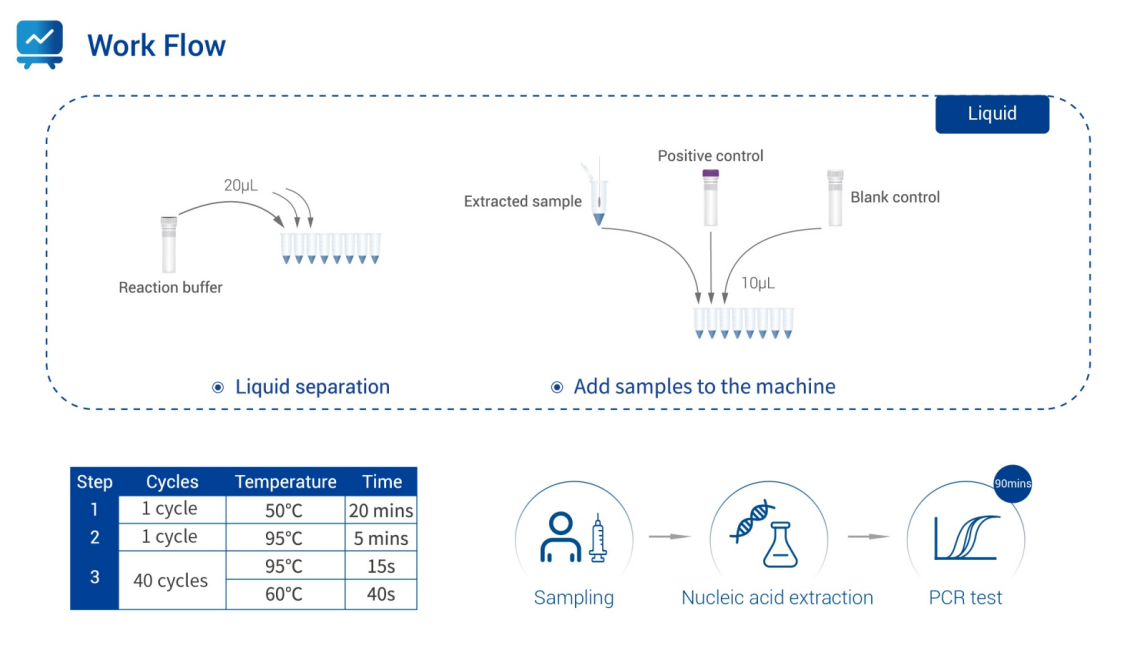
- Оптимізований робочий процес:Має закриту пробірку без попередньої ПЛР-операції, що забезпечує отримання об'єктивних результатів менш ніж за 60 хвилин для пришвидшення прийняття клінічних рішень.
- Операційна гнучкість:Пропонується в рідкому та ліофілізованому форматах для задоволення потреб різних лабораторій.
Прийміть золотий стандарт молекулярного моніторингу. Надайте своїй клініці точність, необхідну для оптимізації довічного догляду за пацієнтами з ХМЛ.Звертайтеся для отримання додаткової інформації:marketing@mmtest.com
Час публікації: 29 вересня 2025 р.
