24 березня 2026 року відзначається 31-й Всесвітній день боротьби з туберкульозом. Всесвітня організація охорони здоров'я (ВООЗ) оголосила цьогорічною глобальною темою«Так! Ми можемо покінчити з туберкульозом!», наголошуючи на тому, що сильне урядове лідерство, стійка політична відданість та скоординовані багатосекторальні дії є важливими для припинення епідемії туберкульозу (ТБ).

Глобальний прогрес та невирішені виклики
Згідно з Глобальною доповіддю про туберкульоз за 2025 рік, глобальна боротьба з туберкульозом досягла значної віхи у 2024 році, як ззниження захворюваності та смертностівперше з часів пандемії COVID-19.
За оцінками10,7 мільйона людейзахворіли на туберкульоз у 2024 році, зокрема у 54% чоловіків, 35% жінок та 11% дітей і підлітків. Серед цих випадків приблизно619 000 (5,8%)були коінфіковані ВІЛ, та390 000 (3,6%)мали мультирезистентний або рифампіцин-резистентний туберкульоз (МР/Риф-ТБ).
ТБ спричинив приблизно1,23 мільйона смертейу 2024 році, залишаючись провідною інфекційною причиною смерті у світі, перевершуючи COVID-19. Після трьох років зростання між 2021 і 2023 роками, глобальна захворюваність на туберкульоз знизилася майже на 2% у 2024 році, що відображає поступове відновлення протитуберкульозних служб.[1]
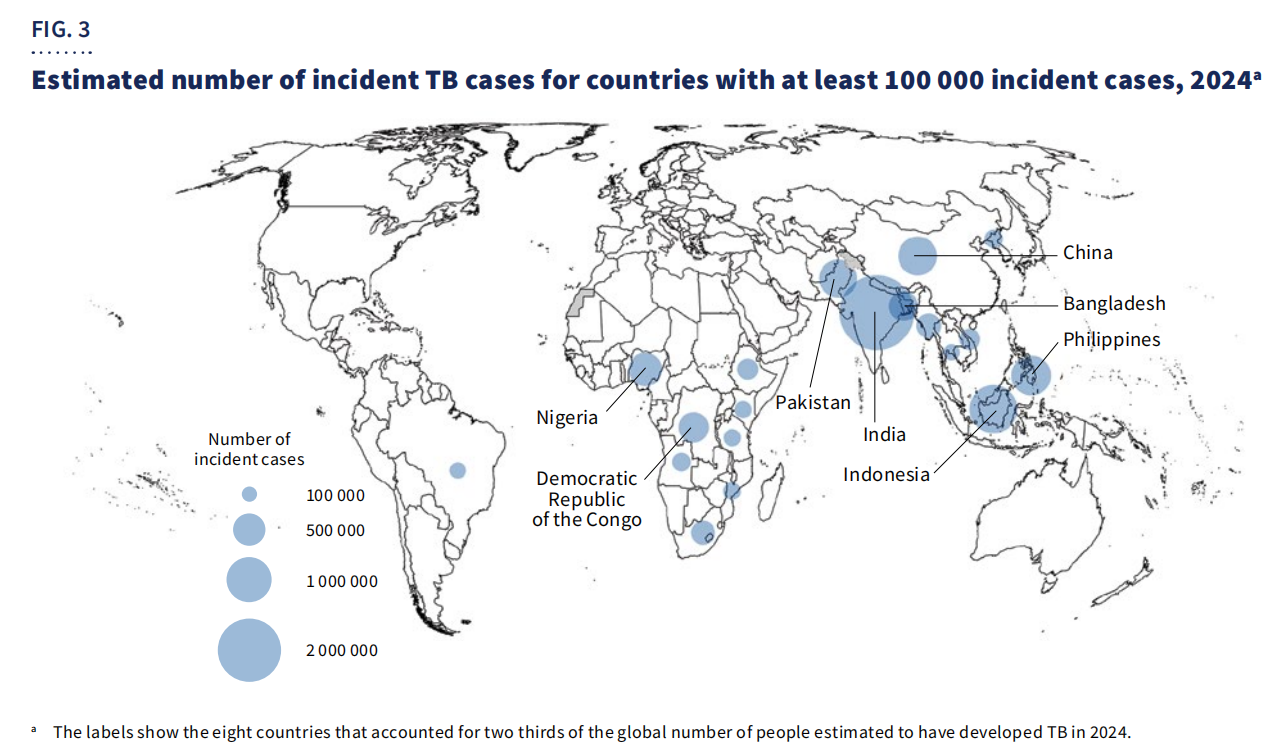
Географічно,67% випадківбули зосереджені у восьми країнах: Індії, Індонезії, Філіппінах, Китаї, Пакистані, Нігерії, Демократичній Республіці Конго та Бангладеш.
Незважаючи на прогрес, туберкульоз залишається провідною причиною смерті серед людей, які живуть з ВІЛ, та одним із головних факторів смертності, пов’язаної з резистентністю до антимікробних препаратів. Глобальне фінансування продовжує бути недостатнім, і лише5,9 млрд доларів СШАдоступні у 2024 році — значно нижчеРічна ціль у розмірі 22 мільярдів доларів СШАвстановлено на 2027 рік.
Ці цифри підкреслюють нагальну потребу зміцнення програм боротьби з туберкульозом у всьому світі, зосереджуючись на розширенні доступу до діагностики, покращенні результатів лікування та усуненні соціальних детермінант, що сприяють передачі туберкульозу. Туберкульоз продовжує потребувати активної міжнародної співпраці та політичної підтримки для досягнення цілей Стратегії боротьби з туберкульозом.
Мікобактерії туберкульозу: патогенез та класифікація
Мікобактерія туберкульозу (MTB/M. tuberculosis) є основним і найпоширенішим збудником туберкульозу (ТБ). Вона може потрапляти в організм людини через дихальні шляхи, травний тракт або пошкоджену шкіру та слизові оболонки, інфікуючи численні органи та викликаючи різні форми ТБ. Легеневий ТБ, який передається переважно крапельним шляхом, становить понад 80% випадків ТБ. До поширених симптомів належать кашель, виділення мокротиння та кровохаркання. Після інфікування легень бактерії можуть поширюватися кровотоком до кількох систем, що потенційно може призвести до ТБ скелета, сечовивідних шляхів або шлунково-кишкового тракту.[2]
МТБ належить до роду Mycobacterium, до якого входять:
- Комплекс мікобактерій туберкульозу (MTBC): включає, серед інших, M. tuberculosis, M. bovis, M. africanum, M. canettii та M. microti. Хоча M. tuberculosis є основною причиною туберкульозу, M. bovis та M. africanum також можуть спричиняти це захворювання.
- Нетуберкульозні мікобактерії (НТМ).
- Мікобактерія лепри, збудник прокази.
Лабораторні діагностичні підходи
Точна та своєчасна діагностика є важливою для ефективної боротьби з туберкульозом. Всесвітня організація охорони здоров'я наголошує, щоТехнології швидкої молекулярної діагностики фундаментально змінили виявлення туберкульозу, дозволивши високочутливу та специфічну ідентифікацію збудників, одночасно виявляючи стійкість до ліків.[1].
- Мікроскопія та культивуванняe: Культуральний метод залишається золотим стандартом діагностики туберкульозу, оскільки він дозволяє остаточно ідентифікувати життєздатні організми та підтримує тестування на чутливість до ліків і геномний аналіз. Однак через повільний темп росту Mycobacterium tuberculosis результати зазвичай потребують 2–8 тижнів, що обмежує його клінічну корисність у терміновому прийнятті рішень.
-Імунологічне тестування: Імунологічні методи, включаючи туберкулінову шкірну пробу (ШТТ) та аналізи вивільнення інтерферону-гамма (IGRA), виявляють імунні відповіді хазяїна на туберкульозну інфекцію. Хоча ці аналізи корисні для виявлення латентної інфекції, вони не можуть надійно розрізняти активну та попередню інфекцію, тому мають обмежену діагностичну специфічність в умовах високого навантаження.
-Молекулярна діагностика (NAAT): ДНК-тести, такі як ампліфікація нуклеїнових кислот (NAAT), рекомендуються через їхню високу чутливість та специфічність.
-Цільове секвенування наступного покоління (tNGS): Технології цільового секвенування забезпечують високоточну ідентифікацію мутацій, пов'язаних з резистентністю. Керівні принципи ВООЗ рекомендують tNGS як передовий інструмент для виявлення резистентності до препаратів після встановлення діагнозу, що підтримує прецизійні стратегії лікування [3].
-Метагеномне секвенування наступного покоління (mNGS): Метагеномне секвенування дозволяє неупереджено виявляти широкий спектр патогенів без попереднього вибору мішені. Цей підхід особливо цінний у складних або неясних клінічних сценаріях, включаючи змішані інфекції та пацієнтів з ослабленим імунітетом, коли традиційна діагностика може бути недостатньою.
ВООЗ також наголошує, що мікробіологічне підтвердження є важливим для початку відповідної терапії та покращення результатів лікування пацієнтів, підкреслюючи важливість інтеграції передової молекулярної діагностики в програми боротьби з туберкульозом [1].
Комплексні рішення для молекулярної діагностики від Macro & Micro-Test
1.Мультиплексна ПЛР-діагностика туберкульозу та лікарської стійкостіТуберкульоз
| Код продукту | Назва продукту | Сертифікація |
| HWTS-RT001 | Набір для виявлення ДНК мікобактерій туберкульозу (флуоресцентна ПЛР) | CE |
| HWTS-RT137 | Набір для виявлення мутацій резистентності Mycobacterium Tuberculosis до ізоніазиду (крива плавлення) | CE |
| HWTS-RT074 | Набір для виявлення резистентності до нуклеїнових кислот та рифампіцину Mycobacterium Tuberculosis (крива плавлення) | CE |
| HWTS-RT102 | Набір для виявлення нуклеїнових кислот на основі ізотермічної ампліфікації ферментативного зонда (EPIA) для Mycobacterium tuberculosis | CE |
| HWTS-RT144 | Набір для виявлення ліофілізованого нуклеїнового комплексу Mycobacterium Tuberculosis (ізотермічна ампліфікація ферментативного зонда) | CE |
| HWTS-RT105 | Набір для виявлення ДНК ліофілізованих мікобактерій туберкульозу (флуоресцентна ПЛР) | CE |
| HWTS-RT147 | Набір для виявлення резистентності до нуклеїнової кислоти Mycobacterium Tuberculosis, рифампіцину та ізоніазиду (крива плавлення) | CE |
Коли є вагома клінічна підозра на туберкульоз (ТБ),HWTS-RT147Тест рекомендується для якісного виявлення інфекції MTB та туберкульозу з множинною лікарською стійкістю (MDR-TB). Цей тест виявляє мутації вген rpoB, що призводить до резистентності до рифампіцину (RIF), та мутацій угени katG та InhA, які пов'язані з резистентністю до ізоніазиду (INH). Він забезпечує ефективний одноразовий тест як на туберкульоз-метаболічний туберкульоз (MTB), так і на туберкульоз-множинну лікарську стійкість (MDR-TB), включаючи внутрішній контроль якості для мінімізації хибнонегативних результатів, забезпечуючи швидкі та точні результати.
2.Цільове секвенування PTNseq для виявлення респіраторних патогенів та профілювання резистентності
| Код продукту | Назва продукту | Специфікація. |
| HWKF-TS0001 | Набір для збагачення генів збудника інфекції кровотоку PTNseq | 24 тести/набір |
| HWKF-TS0002 | Набір для збагачення генів патогенних мікроорганізмів PTNseq для інфекції центральної нервової системи | 24 тести/набір |
| HWKF-TS0003 | Набір для збагачення генів збудника респіраторних інфекцій PTNseq | 24 тести/набір |
| HWKF-AT0003 | Комплект для створення автоматизованої бібліотеки збагачення (ONT) для патогенних мікроорганізмів респіраторних інфекцій PTNseq | 24 тести/набір |
| HWKF-TS0004 | Набір для збагачення генів інфекційних патогенів широкого спектру PTNseq | 24 тести/набір |
| HWKF-TS0005 | Набір для збагачення генів інфекційних патогенних мікроорганізмів надширокого спектру дії PTNseq | 24 тести/набір |
| HWKF-TS0151 | Набір для типування мікобактерій та збагачення генів лікарської стійкості (метод багаторазової ампліфікації) | 24 тести/набір |
У випадках змішаних респіраторних інфекцій (включаючи інфекції верхніх та нижніх дихальних шляхів, туберкульоз та хронічні респіраторні захворювання) або коли потрібен аналіз генів лікарської стійкості (наприклад, підозра на лікарсько-стійкий туберкульоз),Серія PTNseq для цілеспрямованого високопродуктивного виявлення генівможна застосовувати. Заснований на передовій технології цільового секвенування, PTNseq використовує ультрамультиплексну ПЛР для збагачення специфічних цільових послідовностей у поєднанні з високопродуктивним секвенуванням та технологією нанопор третього покоління для комплексної ідентифікації патогенів та профілювання стійкості до ліків.
Система використовує запатентовані високоспецифічні праймери для ультрамультиплексної ампліфікації цільових генів. Завдяки власній базі даних та інтелектуальним біоінформатичним алгоритмам, вона забезпечує точну ідентифікацію патогенів, а також аналіз генів лікарської стійкості та вірулентності. Цільове збагачення зменшує перешкоди від ДНК хазяїна, підвищуючи чутливість у зразках з високим людським фоном та забезпечуючи ефективне виявлення складних мішеней, таких якМікобактерії туберкульозу, гриби, внутрішньоклітинні бактерії, РНК-віруси та гени резистентності або вірулентності.
PTNseq досягає межі виявленнядо 100 копій/млта охоплює175 поширених респіраторних патогенів, включаючи 76 бактерій, 73 віруси, 19 грибів, 7 мікоплазм, а такожХламідіоз, Рикетсіїта 54 гени лікарської стійкостіПанель включаєМікобактерії туберкульозускладні та основні нетуберкульозні мікобактерії.
Серія PTNseq поєднує високу чутливість з економічною ефективністю, покращуючи показники виявлення патогенів та підтримуючи індивідуалізовану антимікробну терапію, одночасно допомагаючи зменшити стійкість до антимікробних препаратів. Інтегрована з повністю автоматизованою системою підготовки бібліотеки секвенування генів (AIOS), вона забезпечує оптимізоване рішення для лікарень з часом обробки від зразка до результату до 6,5 годин.

3. Метагеномне секвенування для виявлення патогенів широкого спектру дії
| Код продукту | Назва продукту | Специфікація. |
| HWKF-MN0011 | Набір для виявлення метагеномних патогенів (DNA-Illumina) | 24 тести/набір |
| HWKF-MN0018 | Набір для виявлення метагеномних патогенів (DNA-MGI) | 24 тести/набір |
| HWKF-MN0021 | Набір для виявлення метагеномних патогенів (DNA-ONT) | 24 тести/набір |
| HWKF-MN0012 | Набір для виявлення метагеномних патогенів (RNA-Illumina) | 24 тести/набір |
| HWKF-MN0019 | Набір для виявлення метагеномних патогенів (RNA-MGI) | 24 тести/набір |
| HWKF-MN0022 | Набір для виявлення метагеномних патогенів (RNA-ONT) | 24 тести/набір |
| HWKF-MN0013 | Набір для виявлення метагеномних патогенів (ДНК+РНК-Illumina) | 24 тести/набір |
| HWKF-AYM0013 | Комплект для автоматизованого створення бібліотеки для виявлення метагеномних патогенів (ДНК+РНК-Ілюміна) | 24 тести/набір |
| HWKF-MN0020 | Набір для виявлення метагеномних патогенів (ДНК+РНК-MGI) | 24 тести/набір |
| HWKF-MN0023 | Набір для виявлення метагеномних патогенів (ДНК+РНК-ONT) | 24 тести/набір |
Коли клінічний діагноз незрозумілий,Виявлення генів патогенів mNGS з високою пропускною здатністюможе бути виконаний на різних зразках пацієнта, включаючи рідину бронхоальвеолярного лаважу, мокротиння, мазки з горла, кров, плевральний випіт, гній та зразки тканин. Цей підхід використовує технологію метагеномного секвенування, де різні зразки проходять цілеспрямовану попередню обробку з подальшою екстракцією нуклеїнових кислот за допомогою скляних кульок та ферментів, що розщеплюють стінки, що підвищує ефективність екстракції. Секвенування адаптовано до кількох платформ, що забезпечує великий обсяг даних для покращення чутливості mNGS та цілісності збірки. Дані аналізуються за допомогою самостійно створеної бази даних та інтелектуальних алгоритмів для виявлення.понад 20 000 патогенів, включаючи бактерії, грибки, віруси та паразити, що надає інформацію про підозрювані патогенні мікроорганізми. Цей метод підходить для пацієнтів із складною діагностикою, критично хворих або пацієнтів з ослабленим імунітетом, включаючи ідентифікаціюМТБскладнийіНТМ, а також змішані інфекції. Це значно покращує показники виявлення патогенів та допомагає направляти клінічне цілеспрямоване використання антибіотиків, що дозволяє точно діагностувати інфекцію.
Висновок
Хоча досягнуто значного прогресу, туберкульоз залишається серйозною глобальною проблемою охорони здоров'я, особливо в контексті лікарської стійкості, дефіциту фінансування та нерівного доступу до діагностики.
ВООЗ наголошує, що розширення доступу до швидкої молекулярної діагностики та передових технологій секвенування є важливим для досягнення цілей Стратегії боротьби з туберкульозом. Завдяки постійним інноваціям, інвестиціям та глобальній співпраці, викорінення туберкульозу вже не є прагненням, а досяжною метою.
Посилання:
- Всесвітня організація охорони здоров’я. Глобальний звіт про туберкульоз 2024/2025: Діагностичне тестування та лікування.
- Всесвітня організація охорони здоров'я. Посібник ВООЗ з вибору молекулярних швидких діагностичних тестів, рекомендованих ВООЗ, для виявлення туберкульозу та лікарсько-резистентного туберкульозу.
- Всесвітня організація охорони здоров’я. Зведені рекомендації ВООЗ щодо туберкульозу: Модуль 3 – Діагностика (оновлення 2024 року).
Час публікації: 24 березня 2026 р.
